-
- 최강조합 '키트루다·엔허투' HER2 양성 위암 1차요법 3상 개시
- HER2 양성 진행성 위암 환자 1차 치료환경에서 항체약물접합체(ADC) 엔허투(Enhertu, 트라스투주맙 데룩스테칸)와 면역항암제 키트루다(Keytruda, 펨브롤리주맙) 병용...
- 2025-04-01
-

- 빅파마의 새 격전지 Lp(a)...릴리의 '레포디시란' 1년↑효과지속
- 심혈관질환 예방을 위한 지질단백질(a)(lipoprotein(a), Lp(a)) 표적치료제 개발을 위한 빅파마간의 경쟁이 치열해는 가운데 릴리는 자사의 치료제 후보 레포디시란...
- 2025-04-01
-
- EU, PTC의 듀시엔형 근이영양증 치료제 '트랜스라나' 승인 취하
- PTC 테라퓨틱스(PTC Therapeutics)의 디스트로핀 유전자의 넌센스 돌연변이형 듀시엔형 근이영양증(nmDMD) 치료제 트랜스라나((Translarna, 성분명 아탈루렌 Ataluren)가 유...
- 2025-03-31
-

- 임핀지, 최초 방광암 수술전후 보조요법 FDA 조기 승인
- 아스트라제네카의 면역항암제 임핀지(Imfinzi, 성분명 더발루맙/durvalumab)가 미국 FDA으로부터 근침윤성 방광암(MIBC) 환자의 수술 전·후 보조요법 적응증으로...
- 2025-03-31
-

- 노보노디스크, 이번엔 경구비만약 후보 판권 확보
- 노보노디스크가 일주일사이 2건의 비만치료제 후보물질 판권을 환보하며 파이프라인 강화에 나섰다.렉시콘 파마슈티컬스(Lexicon Pharmaceuticals)는 28일 자사의 비...
- 2025-03-31
-

- 머크, 아비스코와 피미코티닙 글로벌 판권 계약 체결
- 머크(Merck)가 중국 상하이 소재 아비스코 테라퓨틱스(Abbisko Therapeutics)로부터 건막거대세포종(TGCT, Tenosynovial Giant Cell Tumor) 치료제 후보 피미코티닙(Pimicotinib)의 ...
- 2025-03-31
-

- 사노피, 연 6회SC A·B형혈우병 ‘큐피틀리아’ FDA 승인
- 사노피의 ‘큐피틀리아(Qfitlia, 피투시란/fitusiran)’가 FDA으로부터 A형 및 B형 혈우병을 갖은 12세 이상 소아·성인환자의 예방요법으로 28일 승인받았...
- 2025-03-31
-

- 노바티스 플루빅토, 전이성 전립선암 1차 치료제로 FDA 승인
- 노바티스의 표적 방사성의약품 플루빅토(Pluvicto, 루테튬 루177 비피보타이드 테트라세탄)가 FDA으로부터 전이성 거세저항성 전립선암(mCRPC) 1차요법으로 적응증 ...
- 2025-03-31
-

- 알콘, 오리온 바이오텍 경영권 인수...각막세포치료제 후보 확보
- 안과 전문기업 알콘(Alcon)이 각막내피세포 기능부전으로 인한 수포성각막병증 치료를 목표로 개발된 세포치료제를 보유한 오리온 바이오텍(Aurion Biotech)의 지...
- 2025-03-28
-

- 프레지니우스, 프롤리아·엑스지바 시밀러 FDA 승인
- 프레지니우스카비는 27일 암젠의 프롤리아와 엑스지바(데노수맙 Denosumab) 참조 바이오시밀러 2품목에 대해 FDA 승인을 받았다고 밝혔다.제품명은 프롤리아 참조...
- 2025-03-28
-

- FDA 3500명 등 美복지부, 1만 명 공무원 감원키로
- 미국 보건복지부(HHS)가 FDA, 질병통제예방센터(CDC), 국립보건원(NIH) 등 주요 보건기관을 포함해 총 1만명의 연방 공무원을 감축하는 대규모 조직 개편안을 공식 ...
- 2025-03-28
-
- 친구 하나없는 JAKi...자카비, 펠라브레십과 시너지 효과
- 다재다능하지만 친구하나 없는 JAK억제제 계열 약물로는 처음으로 노바티스의 자카비(룩소리티닙)가 BET 억제제 계열의 펠라브레십(Pelabresib)와 함께, 골수섬유...
- 2025-03-28
-
- MSD, 키트루다SC 3상 첫 공개...FDA 승인결정 9월 23일
- MSD는 면역항암제 키트루다의 피하주사제형(pembrolizumab with berahyaluronidase alfa)의 첫 번째 3상 임상결과를 공개했다. 기존 정맥주사(IV) 제형과 비교해 약동학적 동...
- 2025-03-28
-

- FDA, 프라더-윌리 증후군 첫 치료제 '바이캇' 승인
- 소렌토 테라퓨틱스(Soleno Therapeutics)는 26일 FDA로부터 자사의 희귀질환 치료제 바이캇 XR(Vykat XR(디아족사이드 콜린 diazoxide choline)dl 프라더-윌리 증후군(PWS) 환자...
- 2025-03-27
-
- GSK, 대상포진백신 '싱그릭스' 치매예방 효과 RWE 연구 협업
- GSK는 25일 최근 영국 치매연구소(UK Dementia Research Institute, UK DRI), 보건 데이터 리서치 영국(Health Data Research UK, HDR UK)와 함께 대상포진 백신 싱그릭스가 치매위험 ...
- 2025-03-27
-
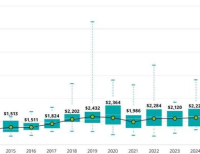
- 글로벌 제약사, 2024년 자산당 평균 신약개발 비용 22억3000만달러
- 2024년 기준 글로벌 제약사의 신약개발 평균 비용은 자산 당 22억3000만달러로 나타났다. 이는 전년도 21억2000만달러에서 1억1000만달러 증가한 수치다. 비용 증가...
- 2025-03-27
-

- 카사바, 알츠하이머 치료제 후보 ‘시무필람’ 개발 공식 중단
- 알츠하이머병 치료제 후보물질로 주목받았던 시무필람(Simufilam)이 끝내 임상 실패로 퇴출 수순을 밟게 됐다. 미국 텍사스에 본사를 둔 카사바사이언스(Cassava Sc...
- 2025-03-27
-

- 타그리소, EGFR 변이 폐암 ADC 등 새 병용전략 가능성 확인
- EGFR 변이를 가진 비소세포폐암 환자를 대상으로 한 아스트라제네카의 타그리소(Tagrisso, 오시머티닙) 기반 병용 전략이 확장되고 있다. 26일부터 체코 프라하에...
- 2025-03-27
- 많이 본 뉴스
-
-
1
한국로슈 발작성 야간 혈색소뇨증(PNH) 희귀질환 신약 ‘피아스카이주’(크로발리맙)’ 국내 허가
-
2
JW중외제약, 리바로 국내 출시 20주년 기념 인포그래픽 공개 … 올 3분기 누적 매출 1413억원, 내년에 ‘리바로페노…
-
3
한국MSD ‘키트루다’, 내년 1월부터 미충족 수요 높았던 소외 암종에 보험급여 확대
-
4
사노피, 주1회 투여 지속형 혈우병A 치료제 ‘알투비오주’ 국내 허가
-
5
크레스콤, 골연령 분석 AI ‘MediAI-BA’ 美 FDA 510K 허가 획득 … 소아 손가락뼈 X-레이를 5초만에 분석
-
6
대한병원의학회 창립, 초대 회장에 신동호 연세대 교수 선출 … 이사장엔 한승준 서울대병원 내과 교수
-
7
한림대 동탄성심병원, 약물 없이 초음파로 알츠하이머 원인 물질 65% 제거
-
8
SK케미칼–넥스트젠바이오사이언스, AI 기반 오픈이노베이션 신약개발 … 후보물질 도출부터 비임상까지 공동 진…
-
9
경북대병원, 비만 환경에서 간암 면역항암치료 저항성 유발 기전 규명
-
10
가톨릭대, 인간 적혈구 기반 비장 표적 생체모사 나노면역치료 플랫폼 개발