글락소스미스클라인(GSK) 한국법인은 PD-1 저해제 ‘젬퍼리주’(Jemperli 성분명 도스탈리맙 dostarlimab)가 지난 14일 식품의약품안전처로부터 국내 허가를 받았다고 16일 밝혔다.
젬퍼리는 면역세포(T세포) 면역관문 수용체인 PD-1을 표적으로 하는 IgG4 인간화 단일클론항체다. 불일치 복구결함 또는 고빈도 현미부수체 불안정(dMMR, DNA Mismatch Repair Deficient/MSI-H, Microsatellite Instability-High, 이하 dMMR/MSI-H) 암종에 지속적인 항종양 활성을 보이는 PD-1 저해제(Programmed Death receptor-1 Inhibitor)다. PD-1은 CD28 계열에 속하는 억제성 면역관문 수용체로서 활성화된 T세포, B세포, NK세포, 골수 계통 세포에서 발현되며, 면역조절에서 중추적인 역할을 수행한다.
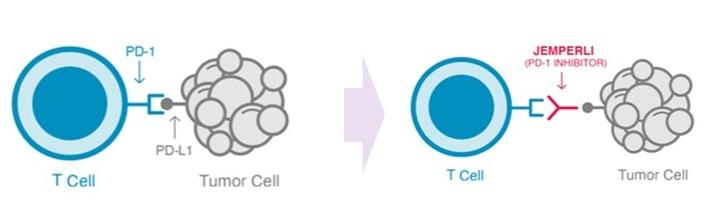 젬퍼리의 작용 기전. 자료 식품의약품안전처
젬퍼리의 작용 기전. 자료 식품의약품안전처
이번 허가로 젬퍼리는 이전 백금기반 전신 화학요법의 치료 중이거나 치료 후 진행을 나타낸 재발성 또는 진행성 dMMR/MSI-H 자궁내막암이 있는 성인 환자에게 사용 가능하다. 젬퍼리는 3주에 한 번씩 4주기(4 cycle) 동안 500mg이 정맥 투여되며 이후부터는 질병이 진행되거나 심각한 독성 발현 시까지 6주마다 1000mg을 투여하게 된다.
자궁내막암은 자궁 체부의 내벽을 구성하는 자궁내막에 생기는 암으로 자궁체부암의 대부분을 차지한다. 대략적으로 자궁내막암 환자 4명 중 1명은 진행성에 해당되거나 재발을 경험하며, 백금기반 항암화학요법 후 질환이 재발했을 때에는 사용할 수 있는 치료법이 제한적이다.
젬퍼리의 허가는 재발성 또는 진행성 고형암 환자를 대상으로 한 다중 코호트1상 임상 GARNET 연구 중, 백금기반 전신 화학요법 도중 또는 이후 진행을 나타낸 재발성 또는 진행성 dMMR/MSI-H 자궁내막암 환자가 등록된 코호트 A1 분석 결과를 기반으로 이뤄졌다. 특히 해당 코호트는 현재까지 진행된 dMMR/MSI-H 자궁내막암 환자에 대한 PD-1 저해제 단독 치료요법 연구 중 규모가 가장 크다.
연구의 1차 평가지표는 독립중앙심사위원회(BICR, Blinded Independent Central Review)가 고형암 반응평가기준(RECIST, Response Evaluation Criteriea Solid Tumors)을 활용해 평가한 객관적반응률(ORR, Objective Response Rate)과 반응지속기간(DOR, Duration Of Response)이었다.
추적 기간 중앙값 16.3개월 기준으로 총 108명의 환자를 분석한 결과, 젬퍼리는 지속적인 항종양 활성과 관리 가능한 안전성 프로파일을 보이는 것으로 확인됐다. 치료에 따른 객관적반응률은 43.5% (95% CI, 34.0-53.4)였으며 반응지속기간은 아직 중앙값에 도달하지 않았다. 질병조절률(DCR, Disease Control Rate)는 55.6% (95% CI, 45.7-65.1)로 나타났으며 치료 반응이 6개월 및 12개월 동안 지속된 비율은 각각 97.9%, 90.9%였다.
자궁내막암 환자 치료에 대한 젬퍼리의 안전성 프로파일은 전체 환자군에 대한 안전성 프로파일과 유사하게 나타났다. 전체 환자군에서 확인된 치료 관련 이상반응(TRAE, Treatment-related Adverse Event)은 대부분 1~2등급에 속했으며 가장 흔하게 보고된 이상반응은 피로(17.6%), 설사(13.8%), 오심(13.8%)이었다.
김재원 서울대병원 산부인과 교수(대한부인종양학회 회장)는 “자궁내막암의 대부분은 조기에 진단돼 상대적으로 예후가 좋지만 초기 환자의 7~15%는 재발을 경험하며 백금기반 항암화학요법 치료 후 재발할 때 사용할 수 있는 치료법이 제한적이었다”며 “다행히 dMMR/MSI-H이 확인된 종양은 PD-1 저해제 치료에 좋은 반응을 보이는데, 유의미한 치료 효과와 안전성 프로파일 및 치료 편의성까지 갖춘 젬퍼리의 허가로 국내 재발성 또는 진행성 dMMR/MSI-H 자궁내막암 2차 치료에 새로운 가능성이 제시됐다”고 말했다.
한국GSK 롭 켐프턴 사장은 “최근 국내 자궁내막암 환자수는 지속적으로 늘어나는 가운데 백금기반 치료 실패 후 재발성 또는 진행성 dMMR/MSI-H 자궁내막암에 대한 치료 옵션이 제한적이었다”며 “국내 자궁내막암 환자와 의료진의 미충족 수요를 해소하고 치료 편의성 및 환자 접근성을 높이기 위해 최선을 다하겠다”고 강조했다.

