 ADC 배경이미지 출처: 삼성바이오로직스항체약물접합체(ACD) 시장이 지난해 130억 달러 규모로 성장했다. 23년 대비 약 30% 가까운 성장세다.
ADC 배경이미지 출처: 삼성바이오로직스항체약물접합체(ACD) 시장이 지난해 130억 달러 규모로 성장했다. 23년 대비 약 30% 가까운 성장세다.
헬스오가 26일 각 제약사의 실적발표를 기반으로 항체약물접합체(ADC) 시장현황을 분석한 결과, 전통강호인 로슈가 매출기준 선두를 유지하고 있는 가운데 23년 ADC 최대매출 품목으로 등극한 엔허투를 앞세운 아스트라제네카와 다이이산쿄 연합이 강력한 추격을 펼치고 있다.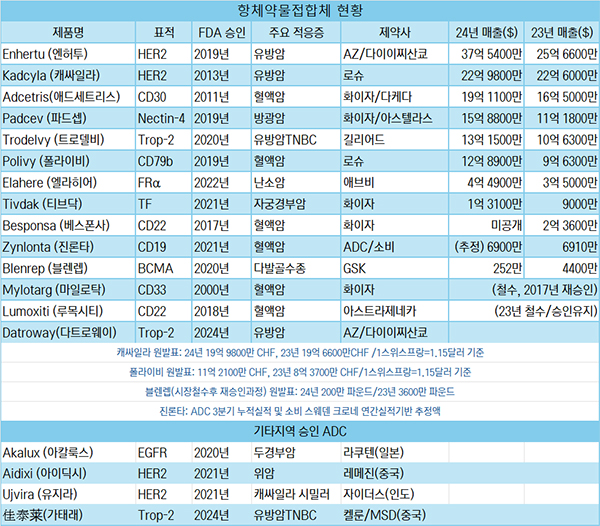 출처 제약사 실적보고 분석정리 헬스오
출처 제약사 실적보고 분석정리 헬스오
로슈의 매출은 캐싸일라와 폴라이비를 더해 45억 달러 규모이며 아스트라제네카와 다이이찌 산쿄의 엔허투는 37억달러 규모다. 아스트라제네카는 올해 HER2 초저발현 유방암까지 적응증 확대한 엔허투와 지난해말 승인된 다트로웨이 까지 라이업을 보강, 선두자리를 노리고 있다.
여기에 더해 23년 말 씨젠(Seagen)을 품은 화이자가 새로운 도전자로 모습을 드러냈다. 가장 많은 품목을 확보, 양강체계를 3강 구도로 전환하는데 성공했다. 또한 ADC의 시작을 알렸지만 미진했던 실적상황을 단숨에 반전시켰다.
승인된 품목수만 보면 애드세트리스, 파드셉, 티브닥, 베스폰사, 마일로탁 등 5품목으로 가장 많다. 4품목 만의 매출이 공개됐는데 36억 달러로 양사에 버금가는 수준이다. PD-1 키트루다와 첫 ADC 조합을 완성한 파드셉이 성장의 중심축을 담당할 것으로 전망된다.
엔허투가 화제의 중심이나 지난해 완성된 3강 구도에서 올해 누가 선두자리를 차지할지 예단이 쉽지 않다.
이밖에 길리어드 역시 트로델비로 한 자리를 차지하고 있는 가운데 애브비가 지난해 초 이뮤노젠(ImmunoGen)을 인수하면서 경쟁에 합류했으며 대표적으로 중국의 켈룬 바이오텍(Kelun biotech)와 협업 등 다양한 협력구조를 통해 MSD 역시 호시탐탐 시장진입을 노리고 있다.
시장에서 잠시 철수했던 GSK 역시 블렌렙의 시장 복귀를 통해 CAR-T와 이중항체가 넘쳐나는 다발성골수종 치료제 시장에서 ADC 약진을 준비중이다. FDA 승인결정예정일은 7월로 잡혀있다.
빅파마의 틈바구니에서 진론타를 보유한 ADC 테라퓨틱스는 스웨덴의 소비(Sobi)와 판권계약을 통한 활로를 모색중이나 3분기까지 누적매출(4분기 실적발표전)은 전년대비 소폭 감소했고 소비의 매출은 미약한 수준이다. 회상명이 ADC이나 후속 ADC 개발에서 적잖은 어려움을 겪으면서 시장에서 존재감을 드러내기는 어려운 상황이다.
전체적으로 FDA 승인 14품목에 더해 중국 2품목, 일본 1품목 등 모두 17품목이 글로벌 시장에서 승인을 받았다. 23년 승인된 ADC는 단 한품목도 없었으나 지난해 다트로웨이와 함께 켈룬의 가태래(MSD 글로벌 판권보유)가 중국 승인을 받아, 2품목이 늘었다. 인도에서 승인된 캐사일라 바이오시밀러까지 포함하면 모두 17개 성분 18품목이다.
올해 승인 가능성이 높은 폼목은 MSD의 파트리투맙 데룩스테칸(Patritumab Deruxtecan)을 꼽을 수 있다. 다이이찌 산쿄로 부터 판권을 확보한 최초의 HER3 표적 ADC로 지난해 6월 FDA로 부터 가속승인신청에 대해 제조시설 문제로 완결된 응답서신(CRL) 통해 승인거부된 바 있다. 다만 3상 성공소식에도 불구 제조시설 문제해결 소식은 전해지지 않고 있다.
이외 MSD의 이피나타맙 데룩스테칸(Ifinatamab Deruxtecan) 등 다수의 후보물질이 3상에 진입했으나 구체적인 결과물은 이른 시점이고 규제승인 신청관련 공식 발표는 없었다.
또한 애브비의 텔리소투주맙 베도틴(Telosotuzumab vedotin)이 승인신청 가능성이 높게 점처지는 가운데 이후 피베키맙 수리닌(Pivekimab sunirine)과 자임윅스(Zymeworks)의 이중항체+약물 접합체 자니다타맙 조보도틴(Zanidatamab zovodotin) 등 1/2상 임상 단계에서 가속승인 가능성이 제시된 품목이 다수 존재한다. 이 역시 규제승인추진 일정은 아직 확인되지 않았다.