-

- 베이진의 PD-1 테빔브라 위암·식도암 1차요법으로 유럽 승인
- 베이진(BeiGene)는 이 자사의 항암제 테빔브라 (TEVIMBRA 티슬렐리주맙, Tislelizumab)가 유럽에서 식도 편평세포암(ESCC)과 위암 또는 위식도 접합부(G/GEJ) 선암의 1차 치...
- 2024-11-28
-

- PTC, 유전자치료제 FDA 승인확보 바우처 2주만에 매각
- PTC테라퓨틱스(PTC Therapeutics) 유전자치료제 FDA 승인을 확보한 소아 희귀질환 우선심사 바우처(PRV)를 1억 5천만 달러에 매각키로 했다. 바우처를 확보한지 단 2주...
- 2024-11-28
-

- 머크, 네르비아노의 PARP1 억제기전 항암제 후보 판권 반환
- 머크는 22년 판권을 확보했던 차세대 PARP1 억제제 후보 NMS-293(NMS-03305293)의 권리를 원개발사인 네르비아노(Nerviano Medical Sciences)사 반환했다.이탈리아에 본사를 ...
- 2024-11-28
-

- 노바티스가 80년전 개발 편두통약 개량신약 FDA 재승인 신청
- 노바티스가 80여년 전에 개발, 승인을 받았던 편두통 치료제의 개량신약에 대한 FDA 재승인신청이 수락됐다.신일본 바이오메디컬(Shin Nippon Biomedical Laboratories/SNB...
- 2024-11-28
-

- 담즙성 담관염 '오칼리바' 결국 유럽 조건부 시판 허가 철회
- 최초의 원발성 담즙성 담관염(PBC) 2차 치료제 '오칼리바'(Ocaliva, 성분명 오베티콜산 Obeticholic Acid)의 유럽 조건부 승인이 결국 취소됐다. 오칼리바의 유럽...
- 2024-11-28
-

- 릴리·노보 호재...바이든 행정부 비만약 26년부터 급여
- 임기 만료을 앞둔 바이든 행정부는 노보노디스크의 위고비(세마글루티드)와 릴리의 젭바운드(터제파타이드/국내 마운자로)의 메디케어·메디케이드 보험...
- 2024-11-27
-

- FDA, 항암제 개발 시 난소 독성 데이터 수집 권고
- FDA는 항암제 개발 시 난소 독성 데이터를 수집하도록 권고하는 초안 지침을 26일 발표했다.지침 초안은 폐경 전 성인을 대상으로 한 항암제 임상시험에서 난소...
- 2024-11-27
-

- 액솜 우울증약 레복세틴 '기면증' 3상 성공 … FDA 승인신청 추진
- 미국 뉴욕의 액솜테라퓨틱스(Axsome Therapeutics, 나스닥 AXSM)는 기면증 치료 신약후보물질인 AXS-12(레복세틴, Reboxetine)가 3상 'ENCORE' 연구에서 주요 평가지표...
- 2024-11-27
-

- 암젠, 월1회 비만약후보 마리타이드 1년 20% 체중감량
- 암젠은 비만치료제 후보 마리타이드(MariTide, maridebart cafraglutide)의 임상 2상 연구에서 긍정적인 결과를 발표했다. 암젠는 26일 마리타이드가 2상(NCT05669599)에서 5...
- 2024-11-27
-

- 로슈, 동종유래 CAR-T세포치료제 개발사 포세이다 인수
- 로슈는 임상단계 생명공학 회사인 포세이다 테라퓨틱스(Poseida Therapeutics)를 약 10억 달러에 인수하기로 확정했다고 26일 발표했다. 포세이다 테라퓨틱스는 캘리...
- 2024-11-27
-

- 로슈, '티쎈트릭+티라골루맙' NSCLC 3상 또다른 실패
- 로슈는 PD-1과 TIGIT 이중 면역항암제 조합인 티쎈트릭(아테졸리주맙)과 티라골루맙(Tiragolumab)의 병용요법 관련 또다른 임상 실패을 전했다.로슈는 26일 PD-L1 수치...
- 2024-11-27
-
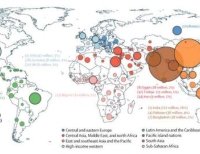
- 2022년 전세계 당뇨병 성인 환자 8억2800만명 … 최다 ‘인도’, 한국은 600만명
- 2022년 전 세계 18세 이상 성인의 당뇨병 유병률이 10%를, 당뇨병 인구가 8억명을 훌쩍 넘은 것으로 조사됐다. 당뇨병 환자는 인구 대국인 인도와 중국만 해도 3억...
- 2024-11-26
-

- 백혈병치료제 글리벡 경구용액 개량신약 FDA 승인
- 아일랜드 소재 쇼올라 온콜로지(Shorla Oncology)의 이매티닙 경구용액 임켈비(IMKELDI 개발명 SH-201)가 25일 FDA 승인을 받았다. 오리지널 품목은 2001년 FDA 승인을받은 ...
- 2024-11-26
-
- MSD, '윈레브에어' 고위험 폐동맥고혈압 3상 성공...적응증 확대 추진
- 엠에스디의 폐동맥고혈압 치료제 윈레브에어 (WINREVAIR, 소타테셉트 sotatercept)가 중증 고위험군까지 적응증 확대를 예고했다.엠에스디는 25일 중증 폐동맥고혈...
- 2024-11-26
-
- AZ, 최초 AKT 억제제 '티루캡' 전립선암 3상서 효과 제시
- 아스트라제네카의 최초의 AKT 억제제 티루캡'(Truqap 카피바서팁, Capivasertib)이 유방암에 이어 전립선암으로 적응증 확대를 예고했다.아스트라제네카는 25일 ...
- 2024-11-26
-

- 바이오하벤의 SMA치료제 후보 3상실패...비만 개발 전환
- 바이오하벤(Biohaven)는 25일 척수성 근위축증(Spinal Muscular Atrophy, SMA) 치료제 후보 탈데프그로베프 알파(Taldefgrobep Alfa)가 3상에서 1차 평가지표를 달성하는데 실패...
- 2024-11-26
-

- 자진철회 ADC 블렌렙 부활 신호탄...FDA 승인신청 수락
- 확증임상의 실패로 시장에서 자진철수했던 GSK의 다발골수종 치료를 위한 항체약물접합체(ADC) 블렌렙(Blenrep 벨란타맙 마포도틴)의 부활의 신호탄을 쏘아 올렸...
- 2024-11-26
-

- '임리직' 후 10년만 항암바이러스 제제 'RP1' FDA 승인신청
- 레플리뮨(Replimune)은 지난 21일 종양용해성 바이러스 치료제 후보 '부솔리모진 오데파렙벡(Vusolimogene oderparepvec, RP1)대해 FDA에 가속승인신청서를 제출했다고 ...
- 2024-11-25
- 많이 본 뉴스
-
-
1
한국로슈 발작성 야간 혈색소뇨증(PNH) 희귀질환 신약 ‘피아스카이주’(크로발리맙)’ 국내 허가
-
2
JW중외제약, 리바로 국내 출시 20주년 기념 인포그래픽 공개 … 올 3분기 누적 매출 1413억원, 내년에 ‘리바로페노…
-
3
한국MSD ‘키트루다’, 내년 1월부터 미충족 수요 높았던 소외 암종에 보험급여 확대
-
4
크레스콤, 골연령 분석 AI ‘MediAI-BA’ 美 FDA 510K 허가 획득 … 소아 손가락뼈 X-레이를 5초만에 분석
-
5
사노피, 주1회 투여 지속형 혈우병A 치료제 ‘알투비오주’ 국내 허가
-
6
대한병원의학회 창립, 초대 회장에 신동호 연세대 교수 선출 … 이사장엔 한승준 서울대병원 내과 교수
-
7
한림대 동탄성심병원, 약물 없이 초음파로 알츠하이머 원인 물질 65% 제거
-
8
SK케미칼–넥스트젠바이오사이언스, AI 기반 오픈이노베이션 신약개발 … 후보물질 도출부터 비임상까지 공동 진…
-
9
경북대병원, 비만 환경에서 간암 면역항암치료 저항성 유발 기전 규명
-
10
가톨릭대, 인간 적혈구 기반 비장 표적 생체모사 나노면역치료 플랫폼 개발