올해 상반기 빅파마의 FDA 승인품목은 급감, 단 5품목에 그쳤다. 전년동기대비
FDA 약물평가 및 연구센터(CDER)올해 상반기 신약 승인은 모두 21품목으로 전년동기 26건 대비 소폭 감소했다. 특히 글로벌매출 상위 50위 이내 빅파마가 내놓은 신약은 단 5품목에 그치며 전년 동기 14품목 대비 64%나 감소했다.
상반기 빅파마의 FDA 승인 5품목은 엠에스디의 폐동맥고혈압치료제 원레비어, 아스트라제네카의 발작성 야간혈색소뇨증 경구치료제 보이데야, 암젠의 소세포폐암치료제 임델트라, 입센의 담즙성간경변증치료제 임델트라, 로슈의 발작성야간혈색소뇨증 치료제 피아스키 등이 전부다.
지난해 동기 FDA 신약승인 품목는 모두 26개. 이중 14품목 빅파마(자체개발/인수합병 및 판권확보품목 포함)으로 비중이 54%에 달했던 것과 비교하면 큰폭의 감소다. 글로벌 상위 10대 제약사로 국한해서도 지난해 7품목에서 3품목으로 비중이 낮아진 것은 동일하다.
상반기 주춤했던 빅파마의 더딘 행보는 하반기 첫 승인 소식을 알린 릴리의 알츠하이머치료제 '도나네맙'으로 시작했으나 하반기에도 크게 달라질 가능성은 없다.
길리어드가 사이마베이 인수로 확보한 셀라델파(Seladelpar), BMS가 카루나 합병으로 확보환 조현병치료제 칼엑스트(KarXT/자노멜린+트로스피움), 아스트라제네카와 다이이찌 산쿄의 TROP2 표적 항체약물접합체(ADC) ‘다토포타맙 데룩스테칸(Dato-DXd) 등이 승인대기 중이다.
또 화이자의 A형과 B형 혈우병치료제 마스타시맙(Marstacimab) 등이 연내 승인이 예상된다. 이외 글로벌 50개사로 포함된 인도 선파마의 JAK억제제 계열 원형탈모치료제 후보 '데우룩소리티닙(Deuruxolitinib) 등을 추가하더라도 지난해 빅파마의 승인건수에 비해 큰 폭의 감소가 예상된다.
한편 상반기 FDA 승인품목 중 가장 관심을 모았던 품목 역시 빅파마의 몫은 아니었다. 최초의 비알콜성지방간염치료제(NASH/대사이상 관련 지방간염(MASH)인 마드리갈의 '레즈디프라'가 가장 높은 화제성을 보인 품목이었다.
국내제약사 보툴리눔 톡신 휴젤의 레티보와 베이진의 PD-1 면역항암제 등을 포함 다른국가의 규제승인이후 FDA 승인을 받은 품목이 유독 많았던 상반기이기도 하다.
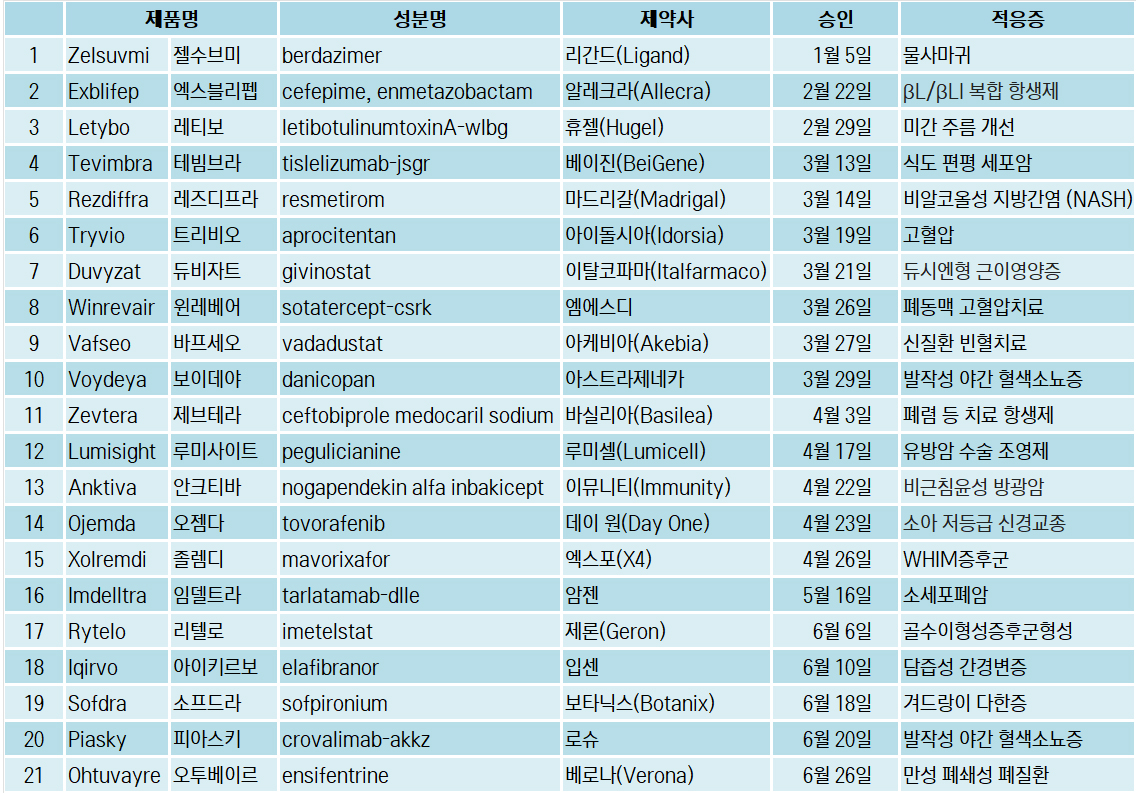
다음은 FDA 승은 21품목 현황이다.