더딘 성장세를 보이는 알츠하이머 치료제 바이오젠과 에자이의 레켐비(레카네맙, 국내 허가), 그리고 새롭게 등장한 릴리의 키순라(Kisunla, 도나네맙)의 성공 방정식의 마지막 해법은 로슈진단이 쥐고 있다.
알츠하이머협회가 지난 6월 27일 새롭게 개정, 발표한 진단 및 병기 분류 기준에 따르면 알츠하이머병을 임상적인 증상에 근거하지 않고 생물학적으로 새롭게 정의하면서 진단의 핵심/비핵심 바이오마커를 설정하고 진단 방법의 통합을 제안했다.
협회는 우선 증상과 관계없이 초기 질환의 유무를 판별하는 핵심 바이오마커로 아밀로이드 베타(Aβ) 플라크와 P-타우(tau 217, 181, 231)의 신경섬유 엉킴을, 두 번째 핵심 바이오마커로는 증상의 악화(병리 설정) 시 측정하는 MTBR-tau243, p-tau205 등을 설정했다.
이외 신경세포 손상과 성상세포의 수준 등은 비핵심 마커로, 혈관뇌손상과 알파-시누클레인의 수준은 다른 질환과 공통의 병리학적 바이오마커로 중요도에 따라 3단계로 세분화했다.
바이오마커를 통한 알츠하이머 진단 방법으로는 양전자 방출 단층촬영(PET)과 뇌척수액(CSF)을 통한 Aβ 42/40 비율, CSF을 통한 p-tau181/Aβ 42, t-tau/Aβ42 비율 등 기존 진단 방법의 병행에 더해 현재 개발 중인 덜 침습적이며 비용이 저렴한 혈액 검사를 통한 플라즈마 바이오마커 검사도 충분한 정확도를 확보할 경우 진단 도구로 활용될 수 있음을 시사했다. 이번 개정의 핵심중의 하나다.
고가의 PET를 당장 완전히 대체할 수는 없으나 점진적으로 진단 방법의 통합을 통해 좀 더 저렴한 진단 옵션을 활용할 가능성을 열어둔 개정 방향이다.
이러한 맥락에서 뇌척수액을 이용한 Aβ 42/40 비율와 pTau 181의 농도를 측정하는 두 가지 FDA 승인 진단 제품은 물론, 가장 저렴한 옵션으로 가능성을 타진하고 있는 혈액 기반 진단 기기(2품목/Aβ, pTau217 측정)의 개발도 모두 로슈진단이 주도하고 있다.
치료제 투약을 위해 PET라는 고가의 장벽을 제거할 수 있는 역할은 로슈가 담당하고 있는 셈이다. PET 진단을 대체할 수 없는 상황에서도 스크리닝을 통해 PET 진단이 꼭 필요한 환자를 특정하거나 또는 보조 역할로 비용 부담을 낮춰 치료 접근성을 높일 수 있다는 점에서도 알츠하이머 치료제의 성장에 감초일 수 밖에 없다.
협회는 병기 분류 기준 중 바이오마커 진단에 따른 분류로 현행 PET 진단 기준 아밀로이드 플라크가 있고 타우 엉킴이 없는 경우 A, 타우 엉킴이 추가될 경우 B, 피질에 타우 침착 시 C, 높은 수준 침착 시 D 단계 등 4단계로 구분지었다.
여기에 대해 잠재적으로 뇌척수액 검사를 통해 A, B, C, D 4단계 진단의 가능성을 소개하고 있다. 예로 CSF Aβ42/40 비율 검사를 통해 비율이 낮으면 아밀로이드 플라크가 있는 것으로 간주되어 A단계로, p-tau181 수준이 높으면 B단계로 간주하는 방식이다. 단, 진단 검사의 정확도가 90% 이상일 경우 뇌척수액 및 혈액 검사를 통한 조기 진단 도구로 활용될 수 있다고 협회는 설명했다.
생물학적 진단 기준 A, B, C, D에 더해 임상적 증상에 따라 0~6단계로 구분했다. 증상은 없으나 다운증후군 등 유전성 알츠하이머병의 우려가 있는 경우 0, 증상이 없으나 바이오마커로 증거가 있는 경우 1, 경미한 인지 기능의 변화 시 2, 초기 인지 장애 3, 기능적 손상의 경증 치매 발생 4, 중등도 치매 5, 심각한 치매 6단계 등이다.
즉, 잠재적 위험은 있으나 무증상 알츠하이머병의 병기를 제외 총 16단계로 병기를 세분화했다. 표로 구성하면 다음과 같다.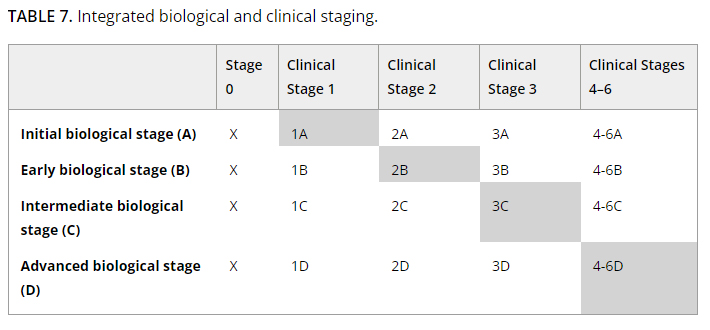
다만, 현재 승인된 레켐비와 키순라가 증상이 발현된 환자에게 승인된 만큼 무증상 환자의 진단은 임상시험 등 연구에만 활용하고 진료 환경에서 진단을 권고하지는 않았다.

