- 문헌재평가 5175품목, 생동성재평가 359품목 … 기한내 입증자료 미제출시 판매정지나 허가취소
식품의약품안전청은 2013년 의약품재평가 대상 품목을 31일 선정·공고했다.의약품재평가는 의약품의 안전성과 유효성을 정기적으로 평가하는 제도로 문헌재평가와 생물학적동등성재평가로 나뉘어 진행된다.
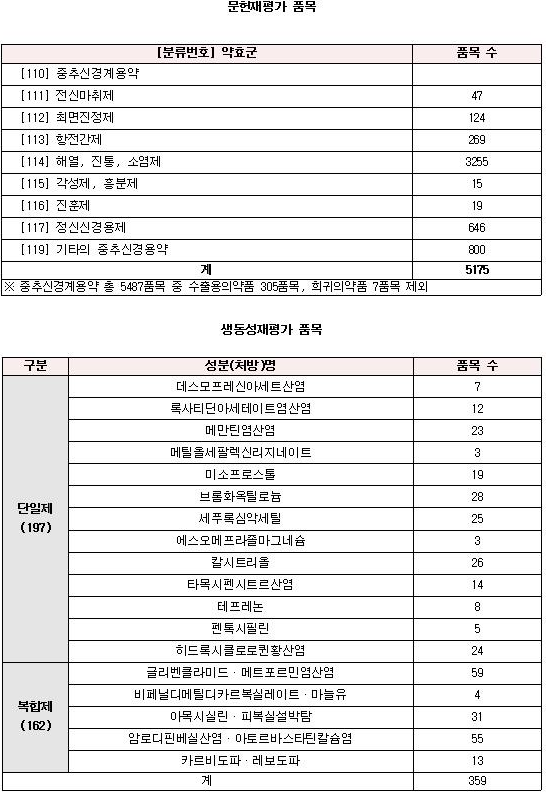
문헌재평가는 중추신경계용약, 전신마취제, 최면진정제, 항전간제, 해열·진통·소염제, 각성·흥분제, 진훈제, 정신신경용제, 기타의 중추신경용약 등 완제의약품 5175품목에 대해 실시된다. 해당업체들은 효능·효과와 용법·용량에 대한 입증자료를 오는 12월 31일까지 식약청에 제출해야 한다. 입증자료가 미흡하거나 외국의 사용현황과 다른 경우 집중 검토품목에 선별되고, 이들 의약품은 내년 4월 30일까지 추가 입증자료를 제출해야 재평가 후 최종결과가 공시된다.
생동성재평가는 지난해 8월 이미 예시한 항생제 ‘세푸록심악세틸’ 등 13개 성분 단일제 197개 품목과 복합제 162개 품목 등 총 359품목을 대상으로 실시된다. 문헌재평가 품목과 마찬가지로 제약사는 생동성시험 계획서를 올 연말까지 제출해야 하고, 생동성시험 결과자료는 내년 6월 30일까지 제출하면 된다.