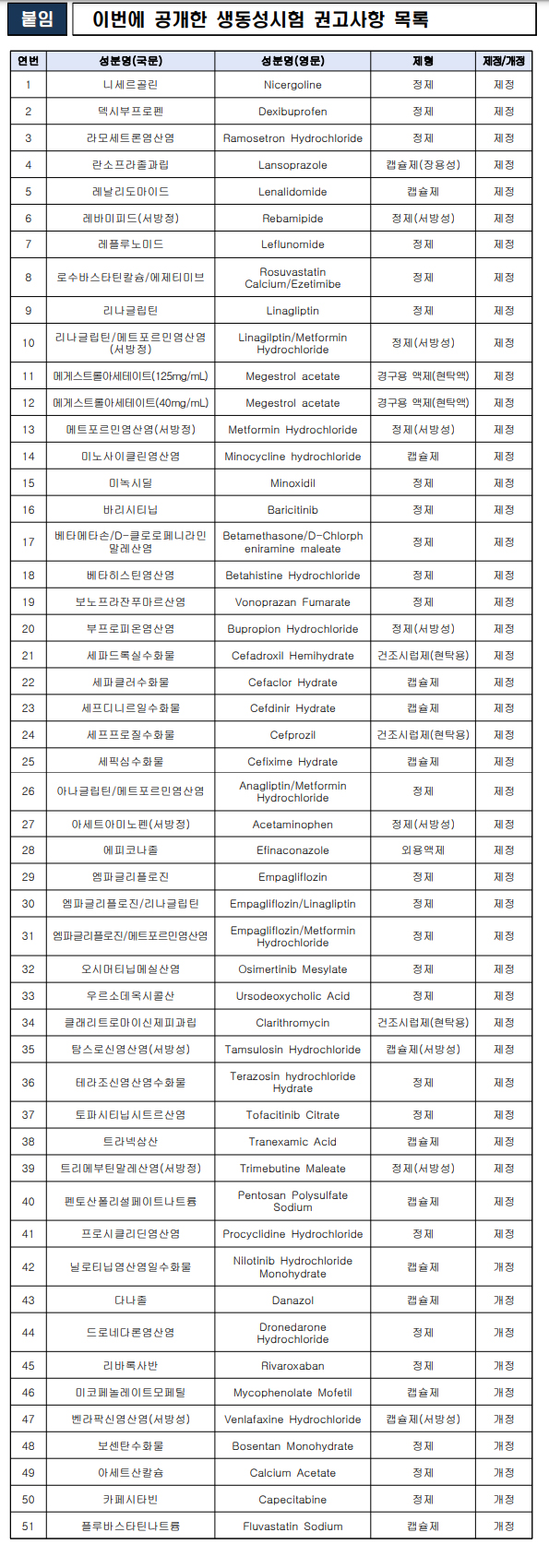
식품의약품안전처는 20일 항암제와 당뇨병 복합제 등을 포함한 51개 품목의 생물학적동등성시험(생동성시험) 권고사항을 새롭게 공개했다고 밝혔다.
식약처는 국내 제약사가 제네릭의약품을 원활하게 개발할 수 있도록 지원하기 위해 시험디자인, 시험대상(필요시 대상자 관리사항 포함), 시험방법(투여방법 및 투여량), 분석 등 생동성 시험을 공개해 오고있으며 이번에 10건을 개정하고 추가로 41건(총 376건)을 공개했다. 주요개정내여용은 생동성 시험중 주의사항, 공복/식후 조건 등이다.
특히 비소세포폐암에 사용되는 표적항암제 오시머티닙메실산염(대조약 타그리소정)은 건강한 성인을 대상으로 하되, 시험 기간 동안 심전도를 모니터링하고 시험 후 피임(남성 4개월, 여성 2개월)하도록 안내하고, 당뇨병복합제는 시험대상자의 안전을 보장하기 위해 혈당 공급(20% 글루코스 수용액제공), 저혈당 모니터링 관리 등을 추가 조치하도록 안내 권고했다.
식약처는 업계가 전자우편(kfdae27@korea.kr)으로 신청하면 생동성시험 관련 정보를 추가로 제공하고 있으며, 앞으로도 생동성시험 권고사항을 지속해서 확대 공개해 나갈 계획이다.
이번에 공개된 생동성시험 권고사항 목록에는 니세르골린(Nicergoline) 정제, 덱시부프로펜(Dexibuprofen) 정제, 라모세트론염산염(Ramosetron Hydrochloride) 정제, 란소프라졸(Lansoprazole) 캡슐제(장용성), 레날리도마이드(Lenalidomide) 캡슐제, 레바미피드(Rebamipide) 서방정, 레플루노미드(Leflunomide) 정제 등이 포함되어 있다.