파킨슨병치료제 ‘ABL301’, 혈액·뇌장벽 통과 … 진행 원인 α-시누클레인 응집체 억제
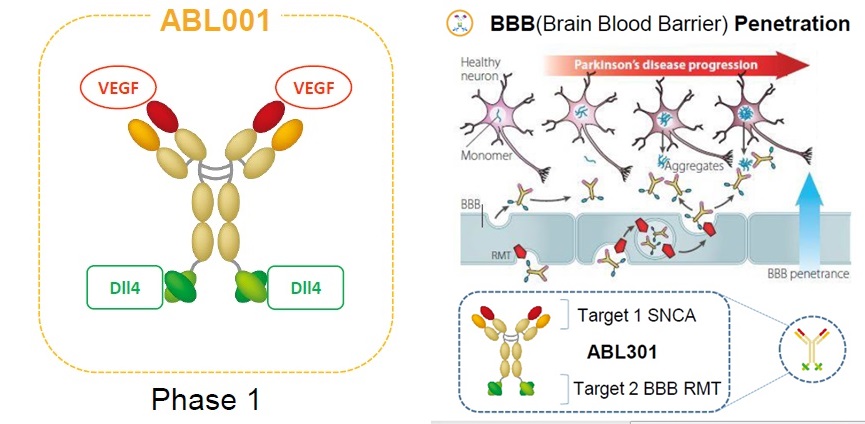
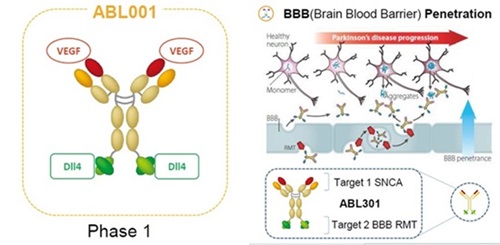 abl바이오의 이중항체 기반 항암 신약후보물질 ‘ABL001’(왼쪽)과 파킨슨병신약 ‘ABL301’의 혈액·뇌장벽(BBB) 통과 기전
abl바이오의 이중항체 기반 항암 신약후보물질 ‘ABL001’(왼쪽)과 파킨슨병신약 ‘ABL301’의 혈액·뇌장벽(BBB) 통과 기전
두 가지 표적물질에 동시에 결합하는 이중항체(bispecific antibody, BsAb) 플랫폼기술이 암과 중추신경계(CNS)질환 신약 상용화의 열쇠로 주목받고 있다.
암·CNS질환은 의약품 시장성이 큰 대표적인 질환군이다. 이중항체 기술은 기존 표적항암제와 접목해 치료반응률을 높인 차세대 신약(best in class)뿐 아니라 새로 발굴한 타깃에 작용하는 혁신신약(first in class) 개발 등 응용 범위가 넓다. 혈액·뇌장벽(BBB, blood-brain barrier) 통과가 가능해 파킨슨병·알츠하이머 치매 등 퇴행성뇌질환의 근본적 치료제 개발에도 활용할 수 있다.
국내에선 ABL바이오가 이 분야에서 가장 앞선 기술을 보유한 곳으로 알려져 있다. 이 회사는 설립된 지 약 2년 밖에 되지 않았지만 한화케미칼 바이오사업부의 신약개발 역량을 그대로 품어 중견 벤처로 여겨진다. 임직원 총 37명 중 32명이 연구원으로 이 중 박사급만 12명에 달한다.
 이상훈 abl바이오 대표
이상훈 abl바이오 대표
이상훈 ABL바이오 대표는 한화케미칼에 합류한 지 약 3년 만인 2016년 초에 한화그룹이 바이오의약품 사업을 접자 창업으로 눈을 돌렸다. 14명의 팀원 모두 그와 뜻을 같이 했다.
이 대표는 “전세계에서 이중항체 관련 유망기술을 보유한 기업은 약 10곳으로 추려진다”며 “우리 회사는 이중항체 기반 의약품 개발에 뛰어든 글로벌 기업인 온코메드(OncoMed), 애브비, 바이오젠, 로슈, 브리스톨마이어스스큅(BMS), 화이자 등과 견줄 만한 차별화된 기술을 갖고 있다”고 말했다.
그는 “이중항체 플랫폼 기술력은 얼마나 새로운(novel) 타깃에 안정적으로 결합할 수 있느냐에서 수준 차이가 난다”며 “우리 회사는 매력적인 신규 타깃을 발굴해 R&D 파이프라인을 확장하고 있다”고 말했다.
이상훈 대표는 “2009년에 유진산 박사와 항체의약품 전문 바이오벤처 파멥신을 공동 창업했던 경험은 지금의 회사를 안정적으로 키울 수 있는 밑거름이 됐다”며 “제넨텍에서 근무하며 신약후보물질 발굴부터 임상 진행까지 항암 항체 연구개발(R&D) 사업 전반을 보는 눈, 사람관리 노하우, 사고 유연성 등을 길렀다”고 덧붙였다.
이 대표는 미국 오하이오주립대에서 분자·세포생물학 박사학위를 받았고, 하버드대·샌프란시스코 캘리포니아대(UCSF) 의대에서 박사후연구원을 지냈다. ‘혁신의 메카’ 미국 실리콘밸리에 있는 카이론(Chiron, 2006년 노바티스에 인수), 아스트라제네카, 제넨텍(로슈 자회사) 등에서 신약개발을 담당했다.
이중항체 항암신약은 암세포와 이를 공격하는 T세포 등 두가지 표적물질에 동시에 결합한다. T세포가 암세포 주위에 모이도록 해 종양 제거 효과가 뛰어나다. 전세계적으로 상용화된 품목은 미국 암젠의 급성림프구성백혈병(ALL) 치료제 ‘블린사이토’(성분명 블리나투모맙, blinatumomab)가 유일하다. 이 약은 암세포 표면의 CD19 단백질과 T세포 표면의 CD3 단백질에 동시에 결합하는 ‘바이트’(Bite)라는 기전을 갖고 있다. 2015년에 미국 식품의약국(FDA)으로부터 시판허가를 받았다.
ABL바이오의 항암 신약후보물질 ‘ABL001’은 지난해 8월 국내 이중항체 의약품 최초로 1a상 임상에 진입했다. 이 후보물질은 혈관내피성장인자(VEGF, vascular endothelial growth factor)와 델타유사체4(DLL4, delta-like 4)에 동시 결합한다. 동물실험 결과 스위스 로슈의 VEGF억제제인 ‘아바스틴’(성분명 베바시주맙, bevacizumab)에 반응을 보이지 않는 환자를 위한 치료제로서 개발 가능성이 확인됐다.
이 대표는 “ABL001은 VEGF나 DLL-4 단일표적 항체를 단독 투여할 때는 물론 이들 항체를 병용투여할 때보다 종양 축소 효과가 뛰어났다“며 “1b상 임상을 진행 중인 온코메드의 VEGF·DLL-4 이중항체 ‘OMP-305B83’과 동물실험 데이터를 비교해도 우월하다“고 말했다.
ABL바이오가 지난 1월 동아에스티에 기술이전한 면역항암제 신약후보물질 2종(‘ABL10X’)은 새로운 표적물질에 결합, 이중항체 중에서도 ABL001보다 기술적으로 한 단계 발전된 형태다. 이들 후보물질은 TNFα수용체 슈퍼패밀리(tumor necrosis factor alpha receptor superfamily)로 분류되는 T세포 관련 보조 면역자극인자(co-stimulator, stimulatory checkpoint molecule)와 암항원(TAA, tumer associated antigen, 암세포 표면 특정 단백질)에 항체의 두 팔이 동시에 붙는다.
이 대표는 “우리 회사의 이중항체 기술은 종양미세환경(tumor microenvironment) 안에서만 T세포를 특이적으로 활성화해 항암 효과와 안전성이 높다”며 “BMS의 ‘옵디보’(성분명 니볼루맙, nivolumab)와 MSD의 ‘키트루다’(펨브롤리주맙, pembrolizumab) 등 기존 PD-1/PD-L1 면역관문억제제에 반응하지 않는 70~80% 암환자를 위한 혁신신약을 개발할 것”이라고 말했다.
ABL바이오가 개발 중인 파킨슨병 신약후보물질 ‘ABL301’은 지난해 11월 세계 과학학술지 ‘네이처’(Nature) 자매지인 ‘바이오파마딜케이커스’(BioPharmaDealmakers)로부터 ‘주목할 만한 뇌질환 파이프라인’으로 꼽혔다.
ABL301 이중항체의 한 팔은 병 진행의 직접적 원인인 알파-시누클레인(α-synuclein, SNCA) 응집체에 결합해 이를 제거하고, 다른 한 팔은 BBB를 통과 하는 기능을 갖도록 디자인됐다. 이 후보물질은 특정 수용체에 결합한 다음 식세포작용(endocytosis)을 통해 뇌 안으로 전달된다.
이 대표는 “ABL301은 캘리포니아대 샌디에이고캠퍼스(UCSD)와 공동 연구한 쥐실험에서 BBB를 통과, α-시누클레인 감소 효과가 확인됐다”며 “호주 교수가 파킨슨병 환자 한 명에게 시험투여한 결과도 긍정적”이라고 전했다.
그는 “ABL301의 수용체 매개 통과세포외배출(RMT, receptor-mediated transcytosis) 기전은 약물의 BBB 통과 방법 중 유일하게 능동적”이라며 “농도차나 펩타이드 부착 등을 이용해 수동적인 기존 방식보다 BBB 투과율이 높을 것으로 기대된다”고 말했다. RMT 기반 NCS치료제를 개발 중인 회사는 알마젠(Armagen)과 제넨텍 등이 대표적이다. 통과세포외배출은 수용체 등 물질을 세포막의 한 측면에서 다른 측면으로 수송하는 식세포작용의 하나다.
abl바이오는 설립 첫해에 한국투자파트너스와 DCS인베스트먼트로부터 총 90억원(시리즈A)을 투자받은 데 이어 지난해 4곳의 기관투자자로부터 총 200억원(각 50억원, 시리즈B)의 투자를 유치했다.
이 대표는 “연내 주식공개상장(IPO, initial public offering)을 추진하고 직원도 총 45명 정도로 늘릴 계획”이라고 말했다. 또 “국내외 여러 제약사와 이중항체 공동연구를 활발히 논의하고 있다”며 “곧 좋은 소식을 전할 것”이라고 귀띔했다.
 abl바이오의 이중항체 기반 항암 신약후보물질 ‘ABL001’(왼쪽)과 파킨슨병신약 ‘ABL301’의 혈액·뇌장벽(BBB) 통과 기전
abl바이오의 이중항체 기반 항암 신약후보물질 ‘ABL001’(왼쪽)과 파킨슨병신약 ‘ABL301’의 혈액·뇌장벽(BBB) 통과 기전  이상훈 abl바이오 대표
이상훈 abl바이오 대표 
