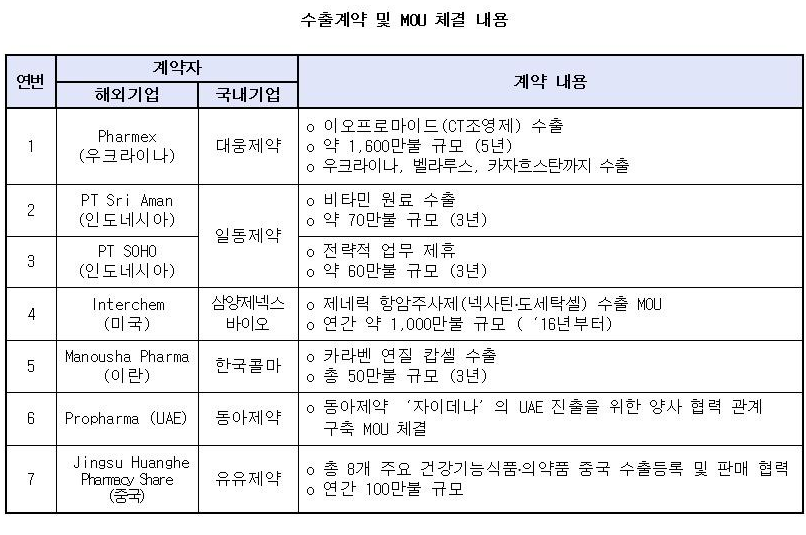
보건복지부와 보건산업진흥원은 14일 일산 킨텍스에서 열린 ‘BIO KOREA 2012’의 ‘팜페어’(Pharm Fair) 행사에서 대웅제약 등 국내 6개 제약사가 중동·동남아·미주·러시아권 등 해외 7개사에 5년간 800억원의 의약품을 수출하는 계약 및 관련 양해각서(MOU)를 체결했다고 밝혔다.
이날 성사된 계약규모는 LG생명과학의 지난해 완제의약품 수출총액에 맞먹고 연간 수출효과로 환산 시 연간 160억원으로 국내 1위 완제의약품 수출품목인 ‘뉴로녹스주’(메디톡신, 보툴리눔톡신 독소A형) 연간수출액의 1.2배, 2위 수출품목(베르나바이오텍, 헤파박스진 및 헤파박스진티에프 주) 연간수출액의 1.6배에 달하는 액수이다.
대웅제약은 이날 행사에서 순수 국내기술로 개발한 컴퓨터단층촬영(CT) 조영제 ‘네오비스트’(성분 이오프로마이드)를 우크라이나, 벨라루스, 카자흐스탄 등 동유럽 3개국과 5년간 1600만달러의 수출 계약을 체결했다. 이 조영제 외에도 독립국가지역(CIS)에 조혈제 ‘에포시스’와 성장호르몬제 ‘케어트로핀’ 등 바이오 제품의 수출 협의를 진행 중이다.
이번 네오비스트의 수출은 지난해 12월 러시아, 지난 2월 이란에 이은 세 번째 해외 시장 진출이다. 대웅제약은 이 성과를 발판으로 미국·유럽·중동·중국 등 다른 해외시장 공략에 박차를 가할 방침이다.
이 회사 서종원 글로벌사업본부장은 “우크라이나 등 동유럽 조영제 시장은 연간 200억원 규모로 연평균 15% 정도의 높은 성장률을 보이고 있다”면서 “이번 수출 계약은 단순한 제품 수출 차원을 넘어 양사간의 파트너십을 공고히 하는데 목적이 있다”고 말했다. 서 본부장은 이어 “이번에 러시아에 이어 동유럽 국가로의 수출을 성사시켜 EU 가입국을 대상으로 수출 국가를 확대하는데 중요한 계기가 될 것으로 기대한다”고 덧붙였다.
국내에서 지난해 8월 발매된 네오비스트는 대웅제약이 특허받은 순수 국내 기술로 자체 개발한 고순도·고수율의 CT 조영제로 불순물 함량이 낮다. 특히 품질기준이 까다로운 미국약전(USP)과 유럽약전(EP)의 품질평가에서 모두 적격 판정을 받아 글로벌 시장에서 통할 수 있는 고품질을 인정받았다.
일동제약은 인도네시아 업체 2곳과 비타민 원료 수출 등 130만달러 규모의 협력 계약을 성사시켰다. 인도네시아의 완제의약품 인·허가규정은 국내와 차이가 있어 완제의약품 수출이 어려운 시장이다. 이에 완제의약품 수출 대신 원료공급 및 기술 수출전략으로 선회해 의약품 원료제공과 현지 생산이 가능하도록 노하우를 제공하는 전략적 제휴 및 원료의약품 수출계약을 성사했다.
한국콜마도 수출 이란 시장의 인·허가제도 등의 정보를 현장 중심으로 파악해 수출계약 성공했다. 이란은 유럽연합(EU)의 GMP를 기본요건으로 하는 높은 수준의 허가기준을 보유하고 있어 필수의약품이나 수입지정의약품이 아닌 경우 수출이 어려웠다. 이에 한국콜마는 ‘수입지정의약품’ 을 중점 수출하는 전략으로 품질이 확보된 약을 50만달러 어치 수출하는 계약을 체결했다.
삼양제넥스바이오는 적절한 파트너를 찾지 못해 미국시장 진출에 곤란을 겪던 중 지난해 품질문제가 발생한 제네릭 항암주사제의 상황을 활용해 인터챔(Interchem)사와 MOU체결을 이끌어 냈다.
동아제약은 아랍에미리트(UAE) 제약기업인 프로파마(Propharma)에서 발기부전치료제 ‘자이데나’에 관심을 보여 공급 협력 및 수출촉진에 대한 MOU를 체결했다.
유유제약은 중국의 보건산업진흥원 수출지원센터의 지원을 받아 중국 유통사인 황하그룹과 매년 약100만달러의 건강기능식품 및 의약품 공급에 대한 계약을 성사했다.
이태한 보건복지부 보건의료정책실장은 “이번 수출 계약 성과는 제약기업들의 글로벌 진출 노력의 성과가 본격적으로 나타나기 시작한 것”이라며 “향후 양국 간 협력을 더욱 긴밀히 해 의약품 개발에 걸친 협력으로 발전하게 하는 계기가 되길 희망한다”고 밝혔다.