지난 3년간 유전자재조합 의약품 신규 임상시험 승인 신청이 지속적으로 늘고, 종류별로는 항체의약품 임상시험 건수가 대다수를 차지했다.
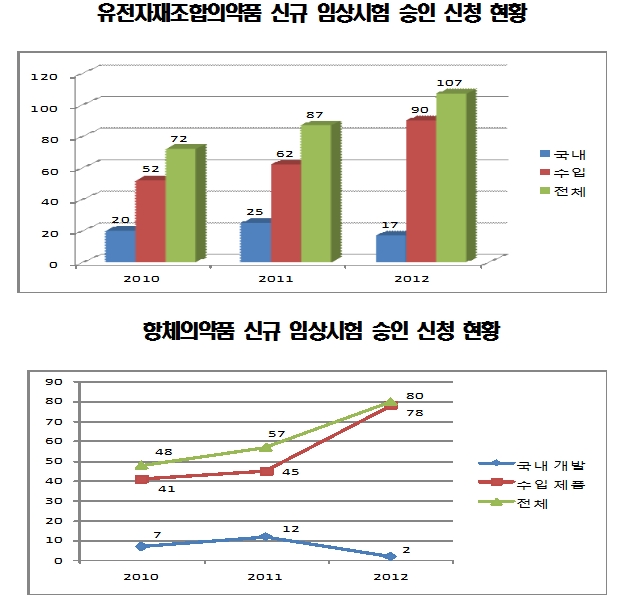
식품의약품안전처가 2010년~2012년 3년간 유전자재조합의약품의 허가 및 임상시험 승인 신청 건수를 분석한 결과 신규 임상시험 승인 신청 건수는 2010년 72건, 2011 87건, 2012년 107건으로 매년 증가한 것으로 나타났다.
수입 제품의 경우 2010년 52건, 2011년 62건, 2012년 90건 등으로 늘었다. 국내 개발은 2010년 20건, 2011년 25건, 2012년 17건으로 조사됐다.
종류별로는 항체의약품의 건수가 2010년 48건으로 67%를 차지했고, 2011년 57건(66%), 2012년에는 80건으로 비중이 75%에 달했다.
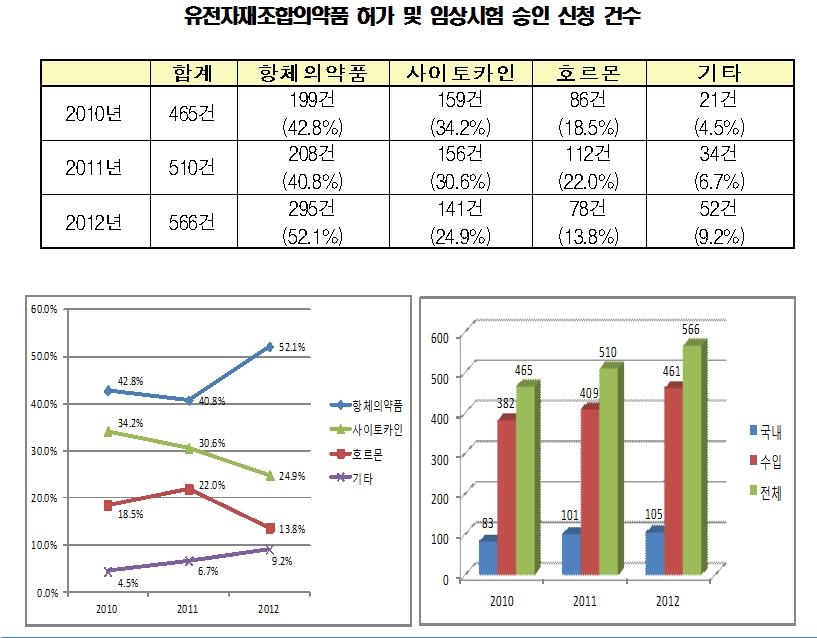
유전자재조합의약품의 허가 및 임상 등 전체 민원 접수 건수는 2010년 465건, 2011년 510건, 2012년 566건으로 매년 지속적으로 증가했다.
수입제품이 2010년 382건으로 82.2%를 점유했고, 2011년 409건(80.2%), 2012년 461건(81.4%)로 대다수를 차지했다.
종류별로는 항체의약품이 2010년 199건으로 43%를 차지했고, 2011년 208건(41%), 2012년 295건(52%)의 비중으로 가장 많았다. 이어 사이토카인, 호르몬제제 등의 순이었다.
항체의약품은 2010년에 항암제와 관절염치료제로 사용되는 것이 대부분이었으나 2011~2012년에는 천식, 골다공증, 치매 등의 효능으로 개발영역이 확대되는 것으로 나타났다.
유전자재조합의약품 중 항체의약품의 개발 비중이 높은 이유는 표적치료가 가능해 선택적 치료효과가 있고 부작용이 합성의약품에 비해 상대적으로 적기 때문이다.
식약처는 이번 조사 결과 유전자재조합의약품 중 개발이 활발한 항체의약품에 대한 지원이 필요하다고 판단하고 올해 하반기에 ‘항체의약품 바이오시밀러의 비임상 및 임상 평가 가이드라인’을 제정키로 했다.
유전자재조합의약품은 유전공학 기술을 이용해 살아있는 세포로부터 생산한 단백질이 주성분이고 종류로는 항체의약품, 사이토카인, 호르몬 제제 등이 있다. 항체의약품은 질환의 원인이 되는 특정 부위에만 결합하는 항체를 유전자재조합 기술로 제조한다.
사이토카인은 호르몬과 작용은 유사하나 다양한 세포에서 분비돼 특정 수용체가 있는 세포에 결합함으로써 작용을 나타내는 물질로서 인터페론, 에리스로포이에틴 등이 있다.
호르몬은 인체 내의 특정 기관에서 분비돼 혈관을 통해 이동해 특정 표적기관에 존재하는 수용체와 결합해 작용을 나타내는 물질로서 성장호르몬, 인슐린 등이 있다.