-
- 트래버, '필스파리' 첫 국소분절 사구체경화증 FDA 신청 추진
- 트래버 테라퓨틱스(Travere Therapeutics)는 면역글로불린A(IgA) 신병증 치료제 필스파리(Filspari, 스파르센탄 Sparsentan)와 희귀 신장질환인 관련 국소분절성 사구체경...
- 2025-02-12
-
- CDK 4/6 억제제 경쟁에서 막내 '버제니오' 주도권 잡았다
- 유방암 치료를 위한 CDK 4/6 억제제 경쟁에서 가장 늦게 출시된 릴리의 버제니오(아베마시클립)이 동일기전 원조제품인 화이자의 입랜스(팔보시클립)의 매출을 ...
- 2025-02-12
-

- FDA, 다발골수종 이중항체 '린보셀타맙' 재승인 신청 수락
- 리제네론은 자사 이중항체 후보 린보셀타맙(linvoseltamab, REGN5458) 관련 FDA 재승인신청이 수락됐다고 11일 밝혔다. 승인결정예정일은 5개월 후인 7월 10일로 잡혔다...
- 2025-02-12
-
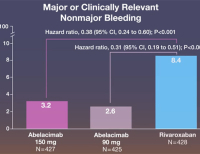
- 노바티스, 위탁개발 F11억제 항응고제 '아벨라시맙' 회수
- 노바티스는 위탁개발을 진행해오던 혈액응고인자 11억제 기전의 항응고제 후보 아벨라시맙(Abelacimab)을 회수한다.노바티스는 11일 미국 보스턴 소재 안토스 테...
- 2025-02-12
-

- 릴리, 어드벤셀과 방사성의약품 개발협업 확대 계약
- 릴리는 호주소재 어드밴셀(AdvanCell)과 다양한 암치료제 개발을 가속화하기 위해 기존 협력을 강화하는 계약을 체결했다.어드밴셀은 10일 기존 계약을 강화한 ...
- 2025-02-11
-

- 애로우·사렙타, 최대 39억달러 규모 판권 및 협업계약 체결
- 애로우헤드 파마슈티컬스(Arrowhead Pharmaceuticals)는 10일 사렙타 테라퓨틱스(Sarepta Therapeutics)와 글로벌 라이선스 및 공동개발 계약을 확정했다고 10일 발표했다.양...
- 2025-02-11
-

- 파드셉·키트루다, 요로상피암 1차요법 혁신적 이점 재확인
- 강력한 임상결과를 기반으로 FDA 승인신청 단 15일 만에 요로상피암 1차 요법으로 승인을 받은 파트셉과 키트루다 조합이 장기추적 연구를 통해 이점을 재확인...
- 2025-02-11
-
- 액솜·테바, 우울증약 '아벨리티' 특허합의...2038년 제네릭 출시
- 액솜 테라퓨틱스와 테바 파마슈티컬스는 우울증치료를 위한 개량신약 아벨러티(AUVELITY, dextromethorphan/bupropion) 관련 특허소송을 종결하고 제네릭 출시일을 2038...
- 2025-02-11
-

- 오페브 후속 폐섬유증 치료제 2번째 3상 성공...규제승인추진
- 베링거인겔하임의 오페브(닌테다닙) 후속 폐섬유증 치료제 후보 네란도밀라스트(nerandomilast / BI 1015550)가 진행성 폐유증 환자 대상 3상에서도 성공했다. 임상결...
- 2025-02-11
-
- 노바티스의 쌍두마차 '코센틱스' 시밀러 첫 中신청 수락
- 노바티스 매출의 쌍두마차 중 하나인 인터루킨-17(IL-17) 억제제 코센틱스(세쿠키누맙)의 첫 바이오시밀러 허가신청이 중국에서 수락됐다.최대 매출품목인 심부...
- 2025-02-11
-
- 로슈, 10년 전 인수 인터뮨 및 에스브리엣 美판권 매각
- 로슈는 10년 전 인수합병한 인터뮨(InterMune)과 특발성 폐섬유증 치료제 에스브리엣(Esbriet, 피르페니돈 pirfenidone)이 미국 판권을 매각했다.케이맨제도 소재에 위...
- 2025-02-11
-
- 애브비, 다제내성 항생제 엠블라베오 FDA 승인
- 애브비는 다제내성 그람음성균 감염 치료제 엠블라베오(EMBLAVEO, 아즈트레오남(Aztreonam)·아비박탐(Avibactam)이 FDA 승인을 받았다고 7일 밝혔다.엠플라베오는 ...
- 2025-02-10
-

- A형혈우병 헴리브라 추격 노보 'Mim8' 소아대상 아쉬운 결과
- A형 혈우병환자를 위한 노보노디스크의 이중항체 피하주사제 후보 Mim8의 소아환자 대상 임상에서는 다소 부족한 임상 결과를 보였다.청소년과 성인환자 대상 ...
- 2025-02-10
-
- 로슈, 혈액암 가싸이바 루푸스 신염 치료효과...규제승인 추진
- 로슈는 자사의 혈액암 치료제 가싸이바(Gazyva 오비누투주맙)의 루푸스 신염 환자대상 긍정적인 3상(REGENCY/NCT04221477))의 세부 임상결과를 7일 발표하고 FDA와 EMA ...
- 2025-02-10
-

- 미국 베인캐피탈, 미쓰비시다나베제약 34억달러(5100억엔)에 인수
- 미국 보스턴 소재 사모펀드 베인캐피털(Bain capital)이 일본제약 7위 기업인 미쓰비시다나베제약을 5100억엔(미화 34억달러, 한화 약 4.9조원)에 인수한다.베인캐피...
- 2025-02-10
-

- 많아도 너무 많은 PD-1...23번째 '안우평' 중국 승인
- 승인을 받은 PD-1 면역관문억제제가 한 품목 더 늘었다. 중국개발 품목으로 13번째고 글로벌 시장 전체에서는 23번째다.중국 베이징 소재 시노셀테크(Sinocelltech/...
- 2025-02-10
-

- 中 헨리우스, 印 닥터레디스와 다잘렉스 시밀러 판권계약
- 중국 상하이 소재 헨리우스(Henlius Biotech)가 다잘렉스(다라투무맙) 바이오시밀러 후보 ‘HLX15’관련 인도소재 닥터레디스(Dr. Reddy’s Laboratories)와 판권...
- 2025-02-07
-

- 강력한 항암라인 힘낸 AZ 541억$ 매출 18% 성장
- 타그리소 임핀지 칼퀀스, 린파자, 엔허투 등 강력한 항암라인을 기반으로 아스트제네카가는 18%의 놓은 성장율을 기록하며 지난해 541억 달러(한화 약 78조원)의...
- 2025-02-07
- 많이 본 뉴스
-
-
1
한국로슈 발작성 야간 혈색소뇨증(PNH) 희귀질환 신약 ‘피아스카이주’(크로발리맙)’ 국내 허가
-
2
JW중외제약, 리바로 국내 출시 20주년 기념 인포그래픽 공개 … 올 3분기 누적 매출 1413억원, 내년에 ‘리바로페노…
-
3
한국MSD ‘키트루다’, 내년 1월부터 미충족 수요 높았던 소외 암종에 보험급여 확대
-
4
크레스콤, 골연령 분석 AI ‘MediAI-BA’ 美 FDA 510K 허가 획득 … 소아 손가락뼈 X-레이를 5초만에 분석
-
5
사노피, 주1회 투여 지속형 혈우병A 치료제 ‘알투비오주’ 국내 허가
-
6
대한병원의학회 창립, 초대 회장에 신동호 연세대 교수 선출 … 이사장엔 한승준 서울대병원 내과 교수
-
7
한림대 동탄성심병원, 약물 없이 초음파로 알츠하이머 원인 물질 65% 제거
-
8
SK케미칼–넥스트젠바이오사이언스, AI 기반 오픈이노베이션 신약개발 … 후보물질 도출부터 비임상까지 공동 진…
-
9
경북대병원, 비만 환경에서 간암 면역항암치료 저항성 유발 기전 규명
-
10
가톨릭대, 인간 적혈구 기반 비장 표적 생체모사 나노면역치료 플랫폼 개발