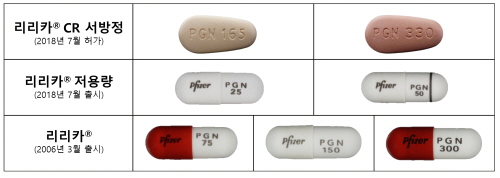
한국화이자제약의 신경병증성 통증치료제 ‘리리카’(성분명 프레가발린, pregabalin)가 지난 18일 식품의약품안전처로부터 서방정 82.5㎎과 165㎎, 330㎎에 대한 판매 허가를 받았다. 프레가발린 성분의 통증치료제 중 서방형 제제로 국내 판매 허가를 받은 약물은 리리카가 처음이다.
이로써 리리카는 지난 7월 1일 출시한 25㎎, 50㎎ 저용량 제제와 더불어 새롭게 허가 받은 CR서방정 제제에 이르기까지 신경병증성 통증 치료에서 다양한 치료옵션을 갖추게 됐다.
‘리리카CR서방정’은 성인의 말초 신경병증성 통증의 치료에 처방된다. 기존 리리카 캡슐의 1일 2회 복용법을 1일 1회로 줄임으로써 환자의 복약 편의성과 순응도를 높일 것으로 기대를 모으고 있다. 허가받은 세 가지 용량 중 165mg과 330mg 두 가지가 먼저 출시된다. 리리카CR서방정은 지난해 10월 미국 식품의약국(FDA)으로부터 당뇨병성 말초신경병증과 연관된 신경병증 통증관리 및 대상포진 후 신경통관리를 위한 치료제로 미국 내 판매 승인을 받은 바 있다 .
한국화이자는 75mg, 150mg, 300mg 세 용량으로 제공되던 기존 리리카 캡슐 제품 라인에 이번 달 1일 25mg과 50mg 저용량 제제를 추가로 출시해 신경병증성 통증 환자의 치료제 선택 범위를 넓혔다.
이 회사 오동욱 대표는 “서방형과 저용량 제제 출시로 신경병증성 통증 질환을 앓고 있는 국내 환자들의 복약 편의성을 높이고, 의료진들에게 다양한 치료옵션을 제공할 수 있게 됐다”며 “리리카는 탄탄한 의학적 근거들을 토대로 신뢰를 쌓아온 오리지널 프레가발린 제제로서 환자들의 치료성적 향상과 삶의 질 개선을 위해 기여할 것”이라고 말했다.
리리카는 섬유근육통 치료제로서 타임지가 선정한 ‘올해의 10대 의학 혁신(Top 10 Medical Breakthroughs)’에 선정된 바 있다. 미국 당뇨병학회(American Diabetes Association) 등이 발표한 당뇨병성 신경병증 통증치료 가이드라인에서 1차 치료제로 우선 권고받는 등 우수성을 인정받았다.

